Тест: 13 вопросов
1.
На иллюстрации изображён гидролиз, конечными продуктами которого являются моносахариды и ортофосфорная кислота. Какие вещества в данном случае подвергаются гидролизу?
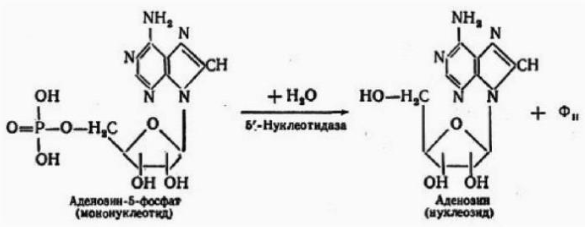
белки
углеводы
жиры
нуклеиновые кислоты
2.
Гидролиз белков – это:
разрушение первичной структуры в водном или щелочном растворе с образованием свободных аминокислот
разрушение первичной и вторичной структуры щелочном растворе с образованием аминокислот
разрушение первичной структуры в водном растворе
разрушение первичной структуры в водном растворе с образованием свободных аминокислот
3.
Гидролиз соли NaCl (хлорид натрия) не происходит, потому что:
она образована нерастворимым основанием
она является нерастворимой
она образована слабой кислотой и слабым основанием
она образована сильной кислотой и сильным основанием
4.
Что из приведённого ниже не усиливает гидролиз?
увеличение концентрации растворённого вещества
увеличения концентрации растворителя
нагревание
связывание продукта в труднорастворимое соединение
5.
Что из приведённого ниже не подавляет гидролиз?
подщелачивание
охлаждение
удаление продукта в газовую фазу
увеличение концентрации растворителя
6.
Алкоголята являются производными спиртов, при гидролизе они распадаются на:
спирты и карбоновые кислоты
спирты
глицерин и соли карбоновых кислот
спирты и щёлочь
7.
Константа гидролиза показывает способность вещества подвергаться электролитической диссоциации. Для каких гидролитических процессов она характерна?
обратимых (по катиону и аниону)
необратимых (по катиону и аниону)
обратимых (по аниону, по катиону)
необратимых (только по катиону)
8.
Продолжите фразу: образованные при гидролизе солей слабые электролиты...
практически мгновенно распадаются ионы
практически не распадаются на ионы
не способны распадаться на ионы
выпадают в осадок и не распадаются на ионы
9.
К специальным случаям гидролиза относиться соль:
NH4NO3
AlCl3
CH3COONa
(NH4)2S
10.
Степень гидролиза – это:
отражение равновесия реакции
совокупность концентрации анионов и катионов
процентное соотношение катионов и анионов
отношение количества подвергшихся гидролизу молекул электролита к общему числу молекул электролита
11.
В 1888 году Вильгельм Оствальд установил закон разбавления веществ, позволявший определять константы диссоциации. Какие количественные показатели гидролиза взаимосвязаны через уравнение Оствальда?
концентрация и растворимость
концентрации анионов и катионов
константа и степень
количество начальных и конечных продуктов
12.
Чтобы избежать хлороза у растений, в почву с пониженной кислотностью вносят (NH4)2SO4. pH почвы снижается благодаря гидролизу:
по аниону
по катиону
по катиону и аниону
зависит от конкретной pH
13.
Ступенчатый гидролиз наблюдается в случае, когда соль образована:
однокислотным основанием или одноосновной кислотой
двухкислотным основанием и двухосновной кислотой
многокислотным основанием или многоосновной кислотой
в любом случае
Для максимально эффективной подготовки к предстоящему зачету или экзамену по химии используйте бесплатное тестирование на нашем сайте. В ходе работы над вопросами теста вы не только проверите свой уровень знаний, но и закрепите изученный ранее материал и обнаружите пробелы, над которыми стоит поработать. Проходите тестирование несколько раз, повторяйте темы и термины, систематизированные специалистами специально для вас.
Заказать решение тестов по химии у экспертов биржи Студворк!



Комментарии